İyonlaşma ve iyonlaşma enerjisi nedir?
 En basit tanımla iyonlaşma; maddeyi oluşturan moleküllerin ya da atomların son enerji seviyesinde yer alan ve çekirdek tarafından “en az çekim kuvvetine maruz kalan” atomun kopartılması ya da yapıya yeni bir elektron dahil edilmesidir. İyonizasyon olarak adlandırılan bu durum, atom veya molekülün bir “iyon” haline gelmesiyle sonuçlanan işlemlerinin tamamında geçerlidir. Maddenin 4 temel halinde biri olan plazma, gaz haldeki maddenin iyonlaşma sürecinden geçmesi sonucunda gerçekleşen ve evrenin her yerinde görülen bir durumdur. İyonize olmuş gazların tamamı, modern fizik ve kimya biliminde “plazma hale geçmiş madde” olarak tanımlanır. Evrende dur durak bilmeksizin gerçekleşen bir atomaltı reaksiyon olan iyonlaşma, maddenin temel yapı birimi olan atomların ya da bu atomların birleşerek oluşturduğu moleküllerin sürekli olarak ısı enerjisine ve basınca maruz bırakılması sonucunda oluşur.
En basit tanımla iyonlaşma; maddeyi oluşturan moleküllerin ya da atomların son enerji seviyesinde yer alan ve çekirdek tarafından “en az çekim kuvvetine maruz kalan” atomun kopartılması ya da yapıya yeni bir elektron dahil edilmesidir. İyonizasyon olarak adlandırılan bu durum, atom veya molekülün bir “iyon” haline gelmesiyle sonuçlanan işlemlerinin tamamında geçerlidir. Maddenin 4 temel halinde biri olan plazma, gaz haldeki maddenin iyonlaşma sürecinden geçmesi sonucunda gerçekleşen ve evrenin her yerinde görülen bir durumdur. İyonize olmuş gazların tamamı, modern fizik ve kimya biliminde “plazma hale geçmiş madde” olarak tanımlanır. Evrende dur durak bilmeksizin gerçekleşen bir atomaltı reaksiyon olan iyonlaşma, maddenin temel yapı birimi olan atomların ya da bu atomların birleşerek oluşturduğu moleküllerin sürekli olarak ısı enerjisine ve basınca maruz bırakılması sonucunda oluşur.
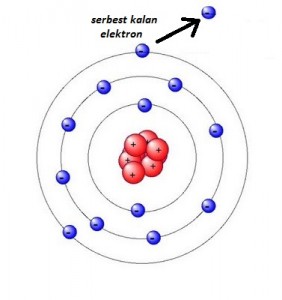
Maddenin hal değiştirmesi yani “faz değişimi” için gaz hale geçen maddenin ısısının daha da fazla arttırılması, belirli bir müddet sonra en az çekime maruz kalan elektronun kopmasına neden olur. Bu durumda serbest kalan elektronlar “serbest elektron uzayı” adı verilen yeni bir uzay meydana getirirken, elektron veren madde de iyonlaşmış olur. İyonlaşma enerjisi de maddenin en az bir elektronunu koparmak için sisteme verilmesi gereken asgari enerji miktarını tanımlamak için kullanılan bir tabirdir. Gaz haldeki maddenin yüksek miktarda ısı enerjisine maruz kalması ve maddeye uygulanan basıncın artması ile elektron koparılması işlemine iyonlaşma dendiği gibi, bu durumun tersi yani maddenin elektron alması da yine iyonlaşma kapsamında incelenmektedir. Zira atom ya da moleküllerin aldığı ve/veya verdiği elektronların elektriksel yükü, iyonlaşma sürecinin de ne şekilde gerçekleştiğini belirler.
 Kopan elektronların elektriksel yükünün artı ya da eksi olmasına göre iyon hale geçen maddenin tanımı da değişir. Elektriksel yükü “artı” olan bir iyonun atom ya da moleküllerindeki elektronun koparılması için maddenin dış ortamdan yüksek miktarda enerji alması gerekmektedir. Isı enerjisine maruz kalan gaz haldeki maddenin en az çekim kuvvetine maruz kalan ilk elektronunun koparılması için gereken enerjiye “1. iyonlaşma enerjisi” denirken, ilk elektronun ardından bir elektron daha koparılması için gereken enerjiye de 2. iyonlaşma enerjisi denmektedir. 1. iyonlaşma enerjisi her zaman 2. iyonlaşma enerjisinden daha düşük olmaktadır. Gaz haldeki bir maddeyi oluşturan atom ya da moleküllerden elektron koparılmaya devam edildikçe maddenin soğurması gereken enerji miktarı, insan aklının sınırlarını zorlayacak biçimde giderek artmaktadır.
Kopan elektronların elektriksel yükünün artı ya da eksi olmasına göre iyon hale geçen maddenin tanımı da değişir. Elektriksel yükü “artı” olan bir iyonun atom ya da moleküllerindeki elektronun koparılması için maddenin dış ortamdan yüksek miktarda enerji alması gerekmektedir. Isı enerjisine maruz kalan gaz haldeki maddenin en az çekim kuvvetine maruz kalan ilk elektronunun koparılması için gereken enerjiye “1. iyonlaşma enerjisi” denirken, ilk elektronun ardından bir elektron daha koparılması için gereken enerjiye de 2. iyonlaşma enerjisi denmektedir. 1. iyonlaşma enerjisi her zaman 2. iyonlaşma enerjisinden daha düşük olmaktadır. Gaz haldeki bir maddeyi oluşturan atom ya da moleküllerden elektron koparılmaya devam edildikçe maddenin soğurması gereken enerji miktarı, insan aklının sınırlarını zorlayacak biçimde giderek artmaktadır.